Descripción
A un tanque de destilación instantánea se alimenta una disolución con la siguiente composición en mol: etano; 8%, propano, 22%; n-butano, 53%; n-pentano, 17%. Si la disolución entra a 13.6 atm y 82°C, ¿Cuál es la cantidad de vapores que puede esperarse y cuál será su composición, si se alimentan 100 kgmol/h?
Referencia: Ejemplo 8 del Barderas. UNAM. Página 39.
Solución.
Componentes: Etano (1); Propano (2); n-Butano (3); n-Pentano (4)
Temperatura: T = 82°C = 179.6°F
Presión: P = 13.6 atm = 199.87 psia
L = ?; xi = ?; yi = ?
Composición de la alimentación: z1 = 0.08, z2 = 0.22, z3 = 0.53, z4 = 0.17
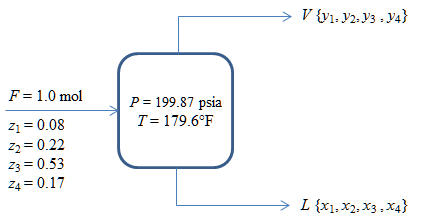
Para averiguar el estado termodinámico de la mezcla se aplica el siguiente criterio:
Utilizar f (V) como indicador preciso.
\( \displaystyle f\,(V)=\sum\frac{Z_i\,(K_i-1)}{1+V\,(K_i-1)}\)
Si f (0) < 0 → Líquido sub-enfriado.
Si f (0) = 0 → Líquido en su Punto de Burbuja.
Si f (1) = 0 → Vapor en su Punto de Rocío.
Si f (1) > 0 → Vapor sobrecalentado.
Si no se cumple alguna de estas condiciones, la corriente será una mezcla de líquido saturado + vapor saturado (Coexistencia de ambas fases en equilibrio).
A P = 199.85 psia y T = 179.6°F, de los diagramas de DePriester:
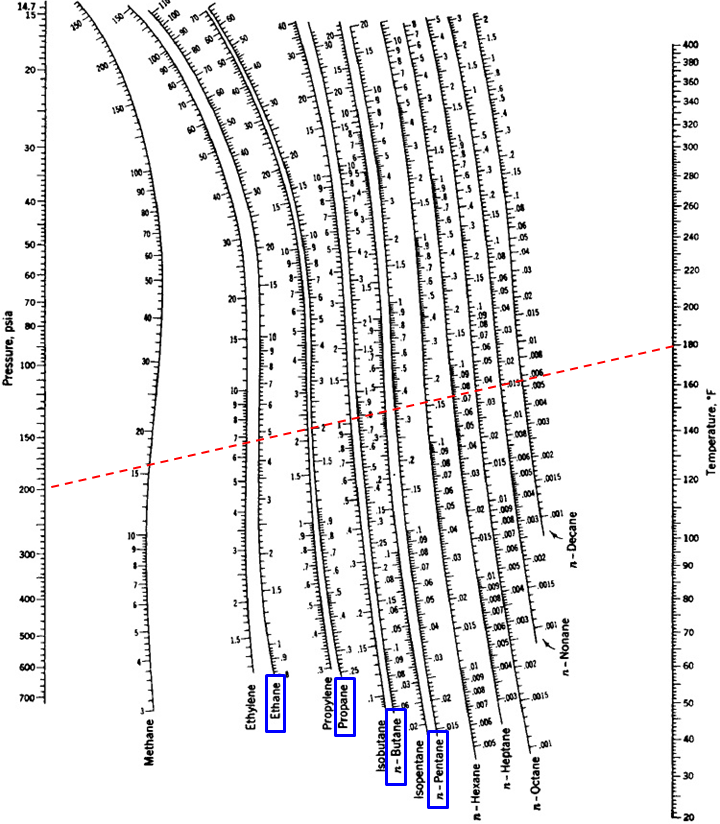
K1 = 4.7; K2 = 2.0; K3 = 0.79; K4 = 0.335
\( \displaystyle f\,(V)=\sum\frac{z_i\,(K_i-1)}{1+V\,(K_i-1)}\)
Para una mezcla de cuatro componentes:
\( \displaystyle f\,(V)=\frac{z_1\,(K_1-1)}{1+V\,(K_1-1)}+\frac{z_2\,(K_2-1)}{1+V\,(K_2-1)}+\frac{z_3\,(K_3-1)}{1+V\,(K_3-1)}+\frac{z_4\,(K_4-1)}{1+V\,(K_4-1)}\)
\( \displaystyle f\,(V)=\frac{0.08\,(4.7-1)}{1+V\,(4.7-1)}+\frac{0.22\,(2.0-1)}{1+V\,(2.0-1)}+\frac{0.53\,(0.79-1)}{1+V\,(0.79-1)}+\frac{0.17\,(0.335-1)}{1+V\,(0.335-1)}\)
\( \displaystyle f\,(V)=\frac{0.296}{1+3.7\,V}+\frac{0.22}{1+V}-\frac{0.1113}{1-0.21\,V}-\frac{0.11305}{1-0.665\,V}\)
Evaluación de las condiciones límite:
f (0) = 0.296 + 0.22 – 0.1113 – 0.11305 = 0.29165 > 0 → Criterio no concluyente.
\( \displaystyle f\,(1)=\frac{0.296}{1+3.7}+\frac{0.22}{1+1}-\frac{0.1113}{1-0.21}-\frac{0.11305}{1-0.665}\)
\( \displaystyle f\,(1)=\frac{0.296}{4.7}+\frac{0.22}{2}-\frac{0.1113}{0.79}-\frac{0.11305}{0.335}\)
f (1) = 0.062979 + 0.11 – 0.140886 – 0.337463 = 0.30537 < 0 → Criterio no concluyente.
Se trata de una mezcla saturada de líquido + vapor en equilibrio.
Cálculo de la fracción de vapor.
f (V) = 0
\( \displaystyle \frac{0.296}{1+3.7\,V}+\frac{0.22}{1+V}-\frac{0.1113}{1-0.21\,V}-\frac{0.11305}{1-0.665\,V}=0\)
Al resolver la ecuación anterior se obtiene: V = 0.4021, por lo tanto, la cantidad relativa de líquido que sale del separador es:
L = 1 – V
L = 1 – 0.4021
L = 0.5979
Cálculo de las composiciones del líquido y el vapor.
Líquido: \( \displaystyle x_i=\frac{z_i}{1+V\,(K_i-1)}\)
\( \displaystyle x_1=\frac{z_1}{1+V\,(K_1-1)}=\frac{0.08}{1+0.4021\,(4.7-1)}=0.032157\)
\( \displaystyle x_2=\frac{z_2}{1+V\,(K_2-1)}=\frac{0.22}{1+0.4021\,(2.0-1)}=0.156907\)
\( \displaystyle x_3=\frac{z_3}{1+V\,(K_3-1)}=\frac{0.53}{1+0.4021\,(0.79-1)}=0.578881\)
\( \displaystyle x_4=\frac{z_4}{1+V\,(K_4-1)}=\frac{0.17}{1+0.4021\,(0.335-1)}=0.232049\)
Vapor: yi = Ki xi
y1 = K1 x1 = 4.7×0.032157 = 0.151138
y2 = K2 x2 = 2.0×0.156907 = 0.313814
y3 = K3 x3 = 0.79×0.578881 = 0.457316
y4 = K4 x4 = 0.335×0.232049 = 0.077736
Resumen:
Fracción de líquido: L = 0.4021 (40.21%).
Composición de las fases en equilibrio:
Líquido: x1 = 0.032157; x2 = 0.156907; x3 = 0.578881; x4 = 0.232049.
Vapor: y1 = 0.151138; y2 = 0.313814; y3 = 0.457316; y4 = 0.077736.
Se producirán 40.21 kgmol de vapores por cada 100 kgmol alimentados. La composición de los vapores, expresada en porcentajes, será: 15.11% de etano, 31.38% de propano, 45.73% de butano y 7.77% de pentano.
Aplicación del Método de Newton para el cálculo de la fracción de vapor.
a) V1 = 0.5
b) \( \displaystyle f\,(V)=\sum\frac{Z_i\,(K_i-1)}{1+V\,(K_i-1)}\)
\( \displaystyle f\,(V)=\frac{0.296}{1+3.7\,V}+\frac{0.22}{1+V}-\frac{0.1113}{1-0.21\,V}-\frac{0.11305}{1-0.665\,V}\)
\( \displaystyle f\,(0.5)=\frac{0.296}{1+3.7\,(0.5)}+\frac{0.22}{1+0.5}-\frac{0.1113}{1-0.21\,(0.5)}-\frac{0.11305}{1-0.665\,(0.5)}\)
f (0.5) = 0.103860 + 0.146667 + (– 0.124358) + (– 0.169363)
f (0.5) = – 0.043194
c) \( \displaystyle f´\,(V)=-\sum\frac{z_i\,(K_i-1)^2}{[1+V\,(K_i-1)]^2}\)
\( \displaystyle f´\,(0.5)=-\frac{(0.103860)^2}{0.08}-\frac{(0.146667)^2}{0.22}-\frac{(-0.124358)^2}{0.53}-\frac{(-0.169363)^2}{0.17}\)
f ´(0.5) = – 0.134835 – 0.097778 – 0.029179 – 0.168729
f ´(0.5) = – 0.430521
d) \( \displaystyle V_2=V_1-\frac{f\,(V_1)}{f´\,(V_1)}\)
\( \displaystyle V_2=0.5-\frac{-0.043194}{-0.430521}\)
V2 = 0.5 + (– 0.100330)
V2 = 0.3997
Las iteraciones siguientes se resumen en la tabla mostrada a continuación:
|
Iteración |
f (V) | f ´(V) | V |
|
1 |
– 0.043194 |
– 0.430521 |
0.3997 |
|
2 |
0.001110 |
– 0.457839 |
0.4021 |
|
3 |
0.000011 |
– 0.456824 |
0.4021 |
Solución: V = 0.4021 moles.


Valoraciones
No hay valoraciones aún.